李健医生的科普号
- 精选 胆囊癌的病因及预防措施
主要参考引用《中华消化外科杂志》2015年11月第14卷第11期指南与共识1主要流行病学危险因素及病因1.1胆囊结石约85%的胆囊癌患者合并胆囊结石。胆囊结石患者患胆囊癌的风险是无胆囊结石人群的13.7倍,在胆囊结石患者中,单个结石直径>3cm者患胆囊癌的风险是直径<1cm者的10倍。1.2胆囊慢性炎症胆囊组织慢性炎症与胆囊肿瘤关系密切。胆囊慢性炎症伴有黏膜腺体内的不均匀钙化、点状钙化或多个细小钙化被认为是癌前病变。胆囊壁因钙化而形成质硬、易碎和呈淡蓝色的瓷性胆囊,约25%瓷性胆囊与胆囊癌高度相关。1.3胆囊息肉胆囊息肉具有恶变倾向的特征如下:(1)息肉直径≥10mm(约1/4发生恶变);(2)息肉直径<10mm合并胆囊结石、胆囊炎;(3)单发息肉或无蒂息肉,且迅速增大者(增长速度>3mm/6个月)。年龄>50岁胆囊息肉患者,恶变倾向增高,需动态观察。1.4胰胆管汇合异常1.5遗传学遗传因素是胆囊癌的常见危险因素,有胆囊癌家族史者,其发病风险增加。基因遗传背景占胆囊结石总发病风险的5%~25%,有胆囊结石家族史者,胆囊癌发病风险亦增加。1.6胆道系统感染慢性细菌性胆管炎明显增加了胆管黏膜上皮组织恶变的风险。常见的致病菌是沙门氏菌(如伤寒沙门氏菌、副伤寒沙门氏菌)和幽门螺杆菌,伤寒带菌者中胆囊癌患病率可增加12倍;幽门螺杆菌携带者的胆囊癌患病率增加6倍。其发病机制可能与细菌诱导胆汁酸降解有关。1.7肥胖症和糖尿病肥胖症者[体质量指数(BMI)>30kg/m2]可明显增加胆囊癌发病率,其BMI每增加5kg/m2,女性患胆囊癌风险增加1.59倍,男性增加1.09倍。肥胖症引起的代谢综合征可增加患胆囊癌的风险,如糖尿病是形成结石的危险因素,糖尿病与结石协同促进胆囊癌的发生[1]。1.8年龄和性别胆囊癌发病率随年龄增加呈上升趋势,20~49岁发病率为0.16/10万;50~64岁为1.47/10万;65~74岁为4.91/10万;>75岁为8.69/10万。此外,女性发病率较男性高2~6倍。建议及推荐:推荐1:为了预防胆囊癌的发生,出现下列危险因素时应考虑行胆囊切除术,且胆囊标本应广泛取材进行病理学检查:(1)直径>3 cm的胆囊结石;(2)合并有胆囊壁不均匀钙化、点状钙化或多个细小钙化的胆囊炎以及瓷性胆囊;(3)胆囊息肉直径≥10 m m;胆囊息肉直径<10 m m合并胆囊结石、胆囊炎;单发或无蒂的息肉且迅速增大者(增长速度>3mm/6个月);(4)合并胆囊结石、胆囊炎的胆囊腺肌症;(5)胰胆管汇合异常合并胆囊占位性病变;(6)胆囊结石合并糖尿病。(推荐等级A级,证据等级I级)推荐2:出现下列情况时,建议间隔6~12个月行彩色多普勒超声动态检查胆囊:(1)胆囊息肉;(2)年龄超过50岁,特别是女性;(3)肥胖症;(4)有胆石症或胆囊癌家族史。(推荐等级A级,证据等级I级)
李健 主治医师 郑大一附院 肝胆胰外科1381人已读 - 精选 原发性肝癌诊疗规范(2017年版)--摘录治疗部分
(一)肝切除术:肝癌的外科治疗是肝癌病人获得长期生存最重要的手段,主要包括肝切除术和肝移植术。1.肝切除术的基本原则:(1)彻底性:完整切除肿瘤,使切缘无残留肿瘤;(2)安全性:保留有足够功能肝组织(具有良好血供以及良好的血液和胆汁回流)以术后肝功能代偿,降低手术死亡率及手术并发症。2.术前肝功能储备的评估:在术前应对病人的全身情况及肝功能储备进行全面评价:常采用美国东部肿瘤协作组提出的功能状态评分(ECOG PS)来评估病人的全身情况;采用Child-Pugh评分、吲哚氰绿(ICG)清除试验37或瞬时弹性成像测定肝脏硬度37-40评价肝功能储备情况;如预期保留肝组织体积较小,则采用CT和/或MRI测定剩余肝的体积,并计算剩余肝体积占标准化肝脏体积的百分比38。一般认为Child-Pugh A级、ICG15<20%-30%是实施手术切除的必要条件;余肝体积须占标准肝体积的40%以上(肝硬化病人),或30%以上(无肝硬化病人)也是实施手术切除的必要条件。3.肝癌切除的适应证:(1)肝脏储备功能良好的Ia期、Ib期和IIa期肝癌是手术切除的首选适应证,尽管有以往研究显示对于直径≤3cm肝癌,切除和射频消融疗效无差异41(证据等级1),但最近的研究显示外科切除的远期疗效更好42-44(证据等级1)。(2)在部分IIb期和IIIa期肝癌病人中,手术切除有可能获得比其他治疗方式更好的效果45,46(证据等级1),但需更为谨慎的术前评估。对于多发性肝癌,相关研究显示,在满足手术安全性的条件下,肿瘤数目≤3枚的多发性肝癌病人可能从手术获益45,47(证据等级1);若肿瘤数目>3枚,即使已手术切除,在多数情况下其疗效也并不优于TACE等非手术治疗。(3)对于其它IIb期和IIIa期肝癌,如有以下情况也可考虑手术切除,如肿瘤数目>3枚,但肿瘤局限在同一段或同侧半肝者,或可同时行术中射频消融处理切除范围外的病灶;合并门静脉主干或分支癌栓者,若肿瘤局限于半肝,且预期术中癌栓可完整切除或取净,可考虑手术切除肿瘤并经门静脉取栓,术后再结合TACE、门静脉化疗或其他全身治疗措施;如合并胆管癌栓且伴有梗阻性黄疸,肝内病灶亦可切除的病人;伴有肝门部淋巴结转移者,切除肿瘤的同时行淋巴结清扫或术后外放射治疗;周围脏器受侵犯,但可一并切除者。此外,对于术中探查不适宜切除的肝癌,可考虑术中肝动脉结扎(已少用,有时用于肝癌破裂出血时的手术止血)和(或)肝动脉、门静脉插管化疗、或术中其他的局部治疗措施等。4. 肝癌根治性切除标准:(1)术中判断标准:①肝静脉、门静脉、胆管以及下腔静脉未见肉眼癌栓;②无邻近脏器侵犯,无肝门淋巴结或远处转移;③肝脏切缘距肿瘤边界>1cm;如切缘< 1cm,但切除肝断面组织学检查无肿瘤细胞残留,即切缘阴性。(2)术后判断标准:①术后2个月行超声、CT、MRI(必须有其中两项)检查未发现肿瘤病灶;②如术前AFP 升高,则要求术后2个月AFP 定量测定,其水平在正常范围(极个别病人AFP降至正常的时间超过2个月)。5.手术切除技术:常用的肝切除主要是包括入肝和出肝血流控制技术、肝脏离断技术以及止血技术。手术技术方面,有经验的医师可开展腹腔镜或机器人辅助微创肝切除术。微创手术具有创伤小和术后恢复快等优点48(证据等级2),但其长期疗效仍需要与传统的开腹手术进行前瞻性的多中心的随机对照研究。经腹腔镜行肝癌切除的指征:①病变位于CouinaudII、III、IVb、V、VI段;②病变大小以不影响第一和第二肝门的解剖为准,一般不超过10cm;③有丰富经验的医师可逐步开展腹腔镜半肝切除、肝3叶切除和CouinaudI、VII、VIII段肝切除。切除范围较大导致余肝体积过少或顾忌余肝的功能,是阻碍根治性切除的主要原因。为了提高肝癌的可切除性,可采用如下方法:(1)术前TACE可使部分病人的肿瘤缩小后再切除49,50;(2)经门静脉栓塞(Portal vein thrombosis,PVE)或门静脉结扎(Portal vein ligation,PVL)主瘤所在半肝,使余肝代偿性增大后再切除51。临床报告其并发症不多,因需4-6周时间等待对侧肝组织体积增大,为减少等待期间肿瘤进展的风险,可考虑与TACE联合52。(3)联合肝脏分隔和门静脉结扎的二步肝切除术(Associating liver partition and portal vein ligation for staged hepatectomy,ALPPS)是近年发展的新技术53,,适合于预期残余肝脏体积占标准肝体积不足30%-40%的病人,经过I期的肝脏分隔或离断和患侧门静脉分支结扎后,健侧剩余肝脏体积(future liver reserve, FLR)一般在1-2周后增生30%-70%以上,FLR占标准肝脏体积至少30%以上,可接受安全的II期切除。术前评估非常重要,需要考虑肝硬化的程度、病人年龄、短期承受两次手术的能力和肿瘤快速进展的风险54;此外可借助腹腔镜技术或消融技术等降低二次手术的创伤55。ALPPS的禁忌证:①存在不可切除的肝外转移灶;②严重的门静脉高压症;③全身麻醉高风险病人以及一般状况较差不能耐受大手术的病人;④I期手术后FLR中有肉眼可见肝癌结节。ALPPS应用可在短期内提高肝癌的切除率,但同时也存在高并发症发生率及死亡率,应谨慎、合理地选择手术对象。(4)对于开腹后探查发现肝硬化较重、肿瘤位置深在、多结节的肿瘤,术中消融可降低手术风险。解剖性切除与非解剖性切除均为常用的手术技术。对于巨大肿瘤,可采用不游离肝周韧带的前径路肝切除法56。对于多发性肿瘤,可采用手术切除结合术中消融(如术中射频等)方式治疗,切除肝脏边缘肿瘤,消融深部肿瘤。对于门静脉癌栓者,行门静脉取栓术时应暂时阻断健侧门静脉血流,防止癌栓播散57。对于肝静脉癌栓或腔静脉癌栓者,可行全肝血流阻断,尽可能整块去除癌栓58。合并右心房癌栓者,可开胸切开右心房取出癌栓,同时切除肝肿瘤。合并腔静脉或右心房癌栓时手术风险较大,应慎重选择。对于肝癌伴胆管癌栓者,在去除癌栓的同时,若肿瘤已部分侵犯胆管壁,则应同时切除受累胆管并重建胆道,以降低局部复发率59。
李健 主治医师 郑大一附院 肝胆胰外科1277人已读 - 就诊指南 胆囊癌的治疗办法
外科治疗原则根治性手术是原发性胆囊癌患者获得治愈可能的唯一方法。胆囊癌的外科治疗应在具有丰富经验的胆道外科医师和病理科医师的医疗中心内完成。手术方式的选择应基于胆囊癌的TNM分期。5.1.1肝切除范围:根据不同T分期的肿瘤入侵肝脏的途径和范围确定肝切除范围,包括肝楔形(距胆囊床2cm)切除、肝S4b+S5切除、右半肝或右三肝切除。(1)Tis或T1a期胆囊癌侵犯胆囊黏膜固有层。此期多为隐匿性胆囊癌,行单纯胆囊切除术后5年生存率可达10%,不需再行肝切除术或二次手术。(2)T1b期胆囊癌侵犯胆囊肌层。由于胆囊床侧胆囊没有浆膜层,肿瘤细胞可通过胆囊静脉回流入肝造成肝床微转移。T1b期肿瘤肝床微转移距离不超过16 m m,故需行距胆囊床2 cm以上的肝楔形切除术[。(3)T2期胆囊癌侵犯胆囊肌层周围结缔组织,未突破浆膜层或未侵犯肝脏。此期胆囊癌细胞经胆囊静脉回流入肝范围平均距胆囊床2~5cm,且至少有一个方向范围>4cm,仅行肝楔形切除术不能达到R0切除,应至少行肝S4b+S5切除术。(4)T3期胆囊癌突破胆囊浆膜层,和(或)直接侵犯肝脏,和(或)侵犯肝外1个相邻的脏器或组织。此期胆囊癌侵犯肝实质主要途径包括:1直接浸润至邻近胆囊床附近的肝实质;2经胆囊静脉途径进入肝脏侵犯肝S4b和S5;3通过肝十二指肠韧带淋巴结经肝门途径沿淋巴管道和Glison系统转移至肝脏。治疗方法包括:1对于T3N0期肝床受累<2cm的胆囊癌,其侵犯肝脏仅有前2条途径而无肝十二指肠韧带淋巴结转移,行肝S4b+S5切除术即可达到R0切除];2对于肝床受累>2cm、肿瘤位于胆囊颈部、侵犯胆囊三角或合并肝十二指肠韧带淋巴结转移者(T3N1期),提示癌细胞沿淋巴管道或Glison系统转移至整个右半肝,需行右半肝或右三肝切除术。(5)T4期胆囊癌侵犯门静脉主干或肝动脉,或2个以上的肝外脏器或组织。有研究结果表明:T4期胆囊癌行扩大根治术,切除率为65.8%,手术组患者5年生存率为13.7%,其中联合肝胰十二指肠切除术后5年生存率为17%;联合门静脉切除重建者1、3、5年生存率分别为48%、29%和6%;非手术组患者5年生存率为0,手术组预后明显优于非手术组(P<0.05)。因而,本指南认为:对T4N0~1M0期胆囊癌患者行联合脏器切除的扩大根治术仍可能达到R0切除,能改善患者预后,肝切除范围为右半肝或右三肝切除。5.1.2淋巴结清扫范围(根据淋巴结受累的路径):术中根据13a组和16组淋巴结活组织检查结果,选择行肝十二指肠韧带淋巴结(12组、8组)清扫术或扩大淋巴结(12组、8组、9组、13组)清扫术。5.1.3肝外胆管处理:术中根据胆囊管切缘活组织检查结果,阳性需联合肝外胆管切除,范围从胰头后上方至第一肝门部,行胆管空肠RouxenY吻合。(1)Tis期或T1a期胆囊癌:单纯胆囊切除即可达R0切除。(2)T1b期胆囊癌:胆囊管切缘活组织检查结果为阴性,无需切除肝外胆管;活组织检查结果为阳性,需行联合肝外胆管切除术。(3)T2期胆囊癌:基于大样本研究结果,不建议常规行肝外胆管切除术。(4)T3期胆囊癌:此期胆囊管未受侵犯时,基于大样本研究结果,不建议对T3期胆囊癌患者行常规肝外胆管切除术。(5)T4期胆囊癌:对于无远处转移(T4N0~1 M0期)的胆囊癌,行胆囊癌扩大根治术仍有望达到R0切除,改善预后,可根据患者情况行联合肝外胆管切除术。5.1.4联合脏器切除及血管重建:T3期和T4N0~1 M0期合并邻近脏器转移的胆囊癌,可行联合受侵犯脏器切除的扩大根治术。(1)T3期胆囊癌合并邻近1个脏器转移,可行联合脏器的扩大根治术。(2)T4期胆囊癌中,T4N0~1M0期患者行根治性手术,术后5年生存率明显优于非手术组患者[31,36]。因而T4N0~1M0期胆囊癌患者行联合脏器切除的扩大根治术仍可能达到R0切除,能改善患者预后。可选择的手术方式包括:联合肝外胆管切除的胆囊癌根治术、联合肝胰十二指肠切除的胆囊癌根治术、联合右半肝或右三肝切除的胆囊癌根治术、联合门静脉切除重建的胆囊癌根治术、联合右半结肠切除的胆囊癌根治术等。非手术治疗胆囊癌目前尚无统一标准的化、放疗方案。基于目前现有的大样本回顾性研究及随机对照临床实验结果,本指南建议以下方案:T1N0期患者的化、放疗:该期患者有统一的研究结果表明:T1N0期胆囊癌患者R0切除术后,行化、放疗组和未行化、放疗组5年生存率比较,差异无统计学意义,故该期患者无需行术后化、放疗。≥T2期,R1切除或淋巴结阳性患者的化、放疗:该期患者行化、放疗能改善总体生存率。(1)化疗:一项多中心III期临床试验研究结果表明:1 12例胆囊癌术后患者给予氟尿嘧啶联合丝裂霉素化疗较未化疗患者5年生存率明显提高(26.0%比14.4%,P<0.05),说明辅助化疗可改善胆囊癌患者的总体预后。另一项回顾性研究纳入103例胆囊癌术后患者,行基于吉西他滨化疗组5年生存率明显优于未行化疗组(57%比24%,P<0.01)。因此,推荐此期患者应行基于氟尿嘧啶或吉西他滨的化疗方案,可改善患者预后。(2)放疗:一项纳入3 0 00例胆囊癌患者的回顾性研究结果表明:17%的患者接受放疗后中位生存时间为14个月,未接受放疗患者中位生存时间为8个月(P<0.05),差异有统计学意义,特别是淋巴结阳性患者(P<0.0 01)或肝脏受累者(P<0.05)。这提示放疗可减缓局部侵犯及提高淋巴结阳性患者的远期生存率。(3)联合化、放疗:回顾性分析17例接受基于氟尿嘧啶联合化、放疗患者的中位生存时间为24个月,与未接受化、放疗患者的1个月比较,差异有统计学意义(P<0.05),多因素回归分析结果表明:联合化、放疗是提高远期生存率的独立预测因素,可明显改善淋巴结阳性患者的预后。
李健 主治医师 郑大一附院 肝胆胰外科2666人已读 - 医学科普 胰腺囊肿怎么办
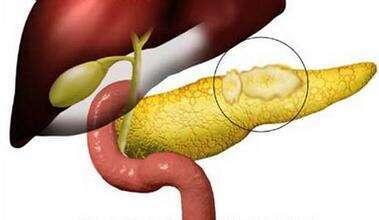
临床上胰腺囊性肿瘤(PCN)的病人越来越多,但外科医师对其认识不深,从而导致了对PCN治疗上的不足或者过度。就PCN当前的国际诊治指南而言,不但存在较多的争议,而且也在不断的修正之中。黏液性囊腺瘤(MCN)及浆液性囊腺瘤(SCN)的诊治策略较为明确,而胰腺导管内乳头状黏液性肿瘤(IPMN)的诊治中存在的争议较多。MRI为PCN首选的非侵入性检查,因其在鉴别诊断上较CT有优势。内镜超声对PCN的诊断敏感性和特异性均较高,是PCN评估的重要组成部分。在治疗上,SCN一般无须手术;而MCN一旦确诊均建议手术切除,若无恶性证据无须术后随访。主胰管型IPMN因恶变率高,一旦确诊应积极手术治疗。分支胰管型IPMN(BD-IPMN)的治疗则存在不少争议,目前国际上对BD-IPMN的治疗总体趋于保守。在手术决策上,肿瘤大小越来越受到重视,肿瘤生长速度及血清CA19-9水平也在近期成为指导BD-IPMN治疗的重要因素。IPMN术后仍存在较高和较长期的复发风险,建议终身随访监测。
 李健 主治医师 郑大一附院 肝胆胰外科2596人已读
李健 主治医师 郑大一附院 肝胆胰外科2596人已读 - 引用 黄疸是怎么回事
什么是黄疸? 黄疸,医学术语又称高胆红素血症,轻度时可能难以发现,最先出现的表现是尿色加深,然后出现眼巩膜泛黄,这时家人或朋友可能会首先发现,问你怎么眼睛黄黄的;然后再出现皮肤黄染,并伴有皮肤瘙痒感,自觉不自觉的挠抓,这就说明你可能有黄疸了。当然,是否真是黄疸,还是血检验最可靠,正常成人血清总胆红素值为3.4~17.1umol/L,其中直接胆红素为0.6~0.8umol/L,间接胆红素为1.7~10.2umol/L。由于巩膜、皮肤、指甲床下和上腭含有较多的弹性蛋白,对胆红素有较强的亲和力,极易黄染。胆红素水平在17~34umol/L之间时,肉眼难以看到巩膜与皮肤的黄染,成为隐形黄疸。当胆红素水平超过34umol/L以上,肉眼可观察到组织黄染,称为显性黄疸。当然,这些数值也只是一个参考,而且各医院检验正常值也可能稍有差异,有时总胆红素值稍微比正常上限高也不一定是病理表现,还需要医生综合全身情况和其它指标来分析才能判断是否黄疸。黄疸是怎么产生的?黄疸只是疾病的表现症状,不是疾病本身,那黄疸到底是怎样产生的呢?我们来了解一下胆红素的来龙去脉吧。人体每日产生250~400mg的胆红素,80%以上来自于衰老红细胞破坏所释放的血红蛋白。红细胞寿命约120天,衰老的红细胞被体内的吞噬细胞系统识别吞噬,释放出血红蛋白,通过分解代谢生成胆红素再释放入血。胆红素进入血液后与清蛋白(相当于快递小哥接活)结合,这种胆红素叫间接胆红素,由清蛋白负责运输到肝细胞膜血窦域再分解游离出胆红素(快递小哥交货给买家——肝细胞),胆红素被肝细胞摄取。在肝细胞的内质网中与葡糖醛酸基转移酶结合成直接胆红素(结合胆红素)(肝细胞内质网加工厂加工一下成为直接胆红素),然后再由肝细胞分泌胆红素进入胆小管,再逐步进入更大一级肝胆管,最后汇集到肝总管经胆总管进入十二指肠,参与食物的代谢过程(小的输送管道输送到大的输送管道一步步集中进入市场)。直接胆红素进入肠道后,又在肠道细菌作用下,还原呈胆素原,大部分随粪便排出体外,并经空气氧化生成棕黄色的粪胆素,是粪便的主要颜色来源。少量胆素原(10%~20%)被肠道黏膜重吸收,经门静脉再回到肝脏,然后大部分又排入肠道,形成胆素原的肠肝循环。小部分随尿排出,尿胆素原被氧化后形成尿胆素,是尿液的主要颜色来源。黄疸的原因?了解了胆红素的来龙去脉之后,我们理解黄疸就容易多了,通俗的原因无非三大方面:胆红素来源过多,发生在胆红素进入肝脏之前,又称为肝前性黄疸,临床最常见的就是溶血性黄疸,红细胞大量破坏,生成的胆红素过多超过了肝脏摄取、结合和排泄的能力,血中间接胆红素浓度增高。肝脏加工不足,属于肝细胞本身功能不足的原因,所以又称为肝细胞性黄疸,最常见的就是所谓的黄疸型肝炎:甲肝、乙肝和丙肝各型肝炎发作都是如此;肝硬化、肝脏肿瘤等损害肝细胞,造成肝细胞对胆红素的摄取、结合和排泄能力降低。胆红素排出障碍,因为是肝脏排出胆红素受阻,发生在肝细胞加工处理之后,又称为肝后性黄疸,也就是广义上的阻塞性黄疸,也称梗阻性黄疸,常见的原因有各种胆管狭窄性疾病、胆道结石、胆管炎、肝脏和胆道肿瘤以及胰头、十二指肠肿瘤等。胆道完全梗阻时,胆红素不能排入肠腔,粪便中因无胆素而呈灰白色似陶土样。出现黄疸怎么办?出现黄疸怎么办,依据黄疸原因不同,诊治的医生分科也不同,例如溶血性黄疸需要看血液科;肝细胞性黄疸往往是消化内科或肝病科;而阻塞性黄疸主要属肝胆外科主治。医学科普不同于其它自然科学知识,即使知道了相关理论知识也不是就能看病的,尽管以上说了那么多黄疸的知识,真正遇到黄疸,估计病友们还是很茫然不知所措的。一个原则就是发现黄疸,毫无疑问看医生!有问题看医生是最正确的做法,并且首先就是找你身边的就近最方便的正规医院医生看,很多问题在当地就能及时解决。即使有些疑难病例一时不能确诊或治疗,当地医生也会给你再往上级医院怎么看提供非常有益的建议,比如该挂哪个科、预计是否需要手术等,然后带上你已做的检查检验资料,按当地医生的建议一步到位挂号诊治。会比你一开始就往大医院跑,毫无目标,挂号不对一个一个科转,反而耽误更多的时间和机会。不正确的做法是自己上网百度或买书看,更不对的就是自己找偏方,这样做可能会耽误疾病的诊治时机,同时也会给自己带来很多不正确的先入为主的观念,甚至会对接诊医生给你的正确建议产生疑问和抵触。本文系冷建军医生授权好大夫在线(www.haodf.com)发布,未经授权请勿转载。
冷建军 主任医师 北京大学首钢医院 肝胆胰外科3.2万人已读 - 就诊指南 2015美国肝胆肿瘤临床实践指南:胆管癌的手术原则
美国国立综合癌症网络关于肝胆肿瘤指南综合了大量的高质量循证医学证据及专家共识,2015 年美国国立综合癌症网络总结出了肝胆肿瘤临床实践指南。美国国立综合癌症网络(NCCN)关于肝胆肿瘤的指南综合大量的高质量循证医学证据及专家共识。在此对 2015 年《NCCN 肝胆肿瘤指南(V2 版)》的要点及临床路径进行转载。根治性手术切除是胆管癌最有效的治疗手段。肝内胆管癌手术原则1. 在进行确定的治疗性手术前进行活组织检查并非必须。在相适的临床特征基础上,影像学显示的可疑肿块应按照恶性病变治疗。2. 应当考虑使用诊断性腹腔镜检查来排除不可切除的扩散性疾病。3. 初始探查应当对多病灶肝病、淋巴结转移及远处转移进行评估。肝门外的淋巴结转移及癌症远处转移是切除的禁忌证。4. 手术治疗的目的是达到阴性边缘的肝切除。为达到切缘阴性,在通常必要的部分切除外,锲状及分段切除均适用的。 5. 肝门淋巴结清扫是合理的,因其可提供分期相关的信息。6. 肝内多灶性病变通常是转移的标志,也是手术切除的禁忌证。在多病灶(有限的)高选择性患者可考虑切除。7. 显著肝门淋巴结转移提示预后不良,仅在高选择性患者中考虑切除。肝外胆管癌手术的原则1. 一般原则(1)手术的基本原则是达到阴性边缘的完全切除及区域淋巴结清扫。这通常需要胰十二指肠切除来处理远端胆道肿瘤,以及肝门肿瘤的主要肝切除,很少通过胆道切除及区域淋巴结清扫术切除中期胆囊肿瘤。(2)应当考虑使用诊断性腹腔镜检查。(3)某些情况下胆管肿瘤累及远端部分胆管,需实施肝切除合并胰胆管切除。这些是不太健全的处理方式,仅在很健康(无显著并发症)的患者中实施。尽管如此,应在适当的临床状态下考虑采用可能的治疗方式。不推荐肝胰腺联合切除时行远端病变淋巴结清扫。2. 肝门胆管癌(1)对可切除性的影像学评估的详细说明超出本指南范围,基本原则是切除肿瘤及其侵犯的胆道支和半侧肝脏,以提高达到切缘阴性的几率,对侧肝脏需要保留完整的动静脉灌注及胆道引流。(2)手术前规划的详细说明超出本指南范围,但需要评估以后的FLR ,且需要评估胆道引流及 FLR 体 积 。在 FLR 较小的患 者(并非所有)中,应当考虑采用 FLR 手术前胆道引流及门静脉侧支栓塞。(3)初始探查应当排除远处转移至肝脏、腹膜及远处淋巴结(超出肝门)这类肝切除的禁忌证,进一步探查必须确定局部的可切除性。(4)从定义上来说,毗邻或已侵袭到肝脏中央区域的肝门区肿瘤需要切除受累的大部分肝脏,包括左右胆管汇合部,通常还需要尾叶切除。(5)门静脉和(或)肝动脉的切除与重建对于完全切除是必需的,而且需要这方面的专家实施。(6)通常采用胆肠 Roux-en-Y 吻合术进行胆道重建。(7)已实施肝门区域淋巴结清扫术。(8)如果可能实施进一步切除,推荐对近端及远端胆道切除再进行冰冻切片评估。远端胆管癌(1)初步评估来排除远处转移病变及局部可切除性。(2)手术通常需要联合经典重建术的胰十二指肠切除术
李健 主治医师 郑大一附院 肝胆胰外科2016人已读 - 就诊指南 2017胆管扩张症(胆管囊肿)诊断与治疗指南----摘录
胆管扩张症,又称胆管囊肿,是临床较少见的一种原发性胆管病变,可由婴幼儿时期先天性胆管扩张延续而来,也可在成年期发病,主要表现为肝内、外胆管单发或多发性局部扩张。对有腹痛、腹上区包块或黄疸等临床表现的患者,尤其是女性患者,鉴别诊断中应考虑胆管扩张症,胆管囊肿可并发胆道结石、急性胆管炎和胰腺炎、胆道癌变等,这是对该病应及时治疗的依据,彩色多普勒超声检查是胆管囊肿的主要筛查手段。 多排螺旋 CT 检查在评估病变胆管周围解剖关系和是否存在并发症上具有优势。 MRCP检查可作为诊断胆管囊肿的首选方法。 胆汁淀粉酶含量检测对判断 PBM具有辅助诊断意义。 血清淀粉酶、胆红素、胆道酶谱(ALP、γGGT)和肿瘤标志物(CA199、CEA)有助于评估 BD 并发症。胆管囊肿一旦确诊,应按照指南制订的治疗原则,尽早行手术治疗,降低胆道癌变率;暂不能行手术治疗者,建议每 6 个月定期随访观察。
李健 主治医师 郑大一附院 肝胆胰外科2166人已读





